En los últimos años, la digitalización y la automatización han transformado numerosos sectores, incluido el ámbito de la salud. Tecnologías como la inteligencia artificial (IA), el aprendizaje automático (ML) y el procesamiento del lenguaje natural (NLP) están transformando las actuales cargas de trabajo que consumen muchos recursos, garantizando un enfoque más informado y eficiente.
El uso de las tecnologías avanzadas en el ámbito de la farmacovigilancia (muy regulada) y cuyo objetivo principal es la monitorización continua de la seguridad de los medicamentos, brinda la oportunidad de innovar mejorado la calidad de los procesos y disminuyendo el tiempo en actividades administrativas y favoreciendo que los profesionales de este ámbito se centren en la evaluación de la seguridad de los medicamentos.
En este artículo se analizan las herramientas y tecnologías emergentes, así como las mejores prácticas para la implementación de soluciones digitales en el ámbito de la farmacovigilancia.
Beneficios de la digitalización y requerimientos de los softwares
Búsquedas bibliográficas
La automatización de las búsquedas bibliográficas ofrece numerosas ventajas en la gestión de la actividad. En primer lugar, la búsqueda automática permite la recuperación de artículos de literatura relevantes utilizando criterios de búsqueda predefinidos y validados, lo que elimina la necesidad de realizar búsquedas manuales y ahorra tiempo al integrar diferentes bases de datos bibliográficas. Esto permite obtener más artículos de interés y reducir la posibilidad de perder información importante de seguridad. El uso de tecnologías avanzadas, como la IA, puede facilitar la clasificación de artículos según su contenido, analizando de forma automática el texto resumen o el texto completo de los artículos, para determinar si contiene información relevante de seguridad.
Triage de casos
El triage y la introducción de RAs en una base de datos de farmacovigilancia puede rentabilizarse mediante la automatización de diferentes etapas del proceso. Esto incluye la transferencia automática de datos desde cualquier tipo de fuente escrita u oral con diferentes formatos (CIOMS I o similares, correos electrónicos, grabaciones telefónicas etc.). Las técnicas de NLP identifican automáticamente y de manera rápida reacciones adversas en el documento fuente y permiten la codificación MedDRA, la evaluación automática de la de causalidad y la gravedad de la RA identificada. La clave para este proceso está en estudiar la compatibilidad del software con la base de datos de la compañía para vincularlos correctamente.
Regulatory Intelligence
Existen softwares diseñados para revisar los sitios web de agencias reguladoras en busca de actualizaciones publicadas diariamente sobre alertas de seguridad y actualizaciones de legislación. Estos softwares seleccionan automáticamente la información publicada de interés reduciendo el tiempo empleado en una búsqueda manual y evitando errores en la selección. De esta manera, facilitan la toma de decisiones informada sobre la seguridad de los productos.
Screening de Redes sociales
Actualmente, en el ámbito de la farmacovigilancia, es un requisito monitorizar las páginas esponsorizadas por la compañía en busca de información relevante sobre la seguridad de sus productos. Sin embargo, cada vez es más frecuente y recomendable ampliar este análisis para abarcar todo internet y todas las redes sociales de acceso libre. Este cambio reconoce la creciente influencia de las redes sociales como nueva fuente de información de seguridad pública y la captura de posibles RAs. Un software de automatización para el screening de redes sociales orientado a farmacovigilancia ofrece una solución eficaz para rastrear y analizar una gran cantidad de publicaciones en tiempo real. Además, permite obtener informes automáticos en los que se puede observar las tendencias de las menciones del producto por país y fuente, y compararlo con otros.
Detección de señales
El proceso de detección de señales implica analizar datos sobre el uso del producto, para detectar cualquier información nueva de seguridad con el fin de identificar nuevas evidencias que indiquen una posible asociación entre la administración del producto y un evento específico reportado. Las herramientas estadísticas avanzadas con IA y data science llevan a cabo la detección de señales multimodal que consiste en combinar las estadísticas de las diferentes fuentes de datos disponibles para generar una puntuación de señal más precisa. Además, permite realizar un análisis específico de situaciones especiales, como el uso de productos en poblaciones sensibles.
Aspectos generales
Por otro lado, independientemente del tipo de software que estemos valorando, es esencial que cumpla con una serie de requisitos:
Primero, debe estar validado y contar con un sistema de audit trail que registre todas las acciones y modificaciones realizadas en el sistema. También es importante que el software permita trabajar con diferentes entornos, de modo que cada usuario tenga acceso a un espacio de trabajo personalizado y adaptado a sus necesidades específicas. El acceso restringido es un requisito clave para la trazabilidad, así como un sistema de copias de seguridad que garantice la recuperación de los datos en caso de pérdida o ataque informático.
El software debe contar con una garantía de cumplimiento de licencias y un mantenimiento continuo que asegure que el software siga siendo compatible con las últimas tecnologías y normativas, y que los usuarios reciban el soporte necesario para garantizar un funcionamiento óptimo.
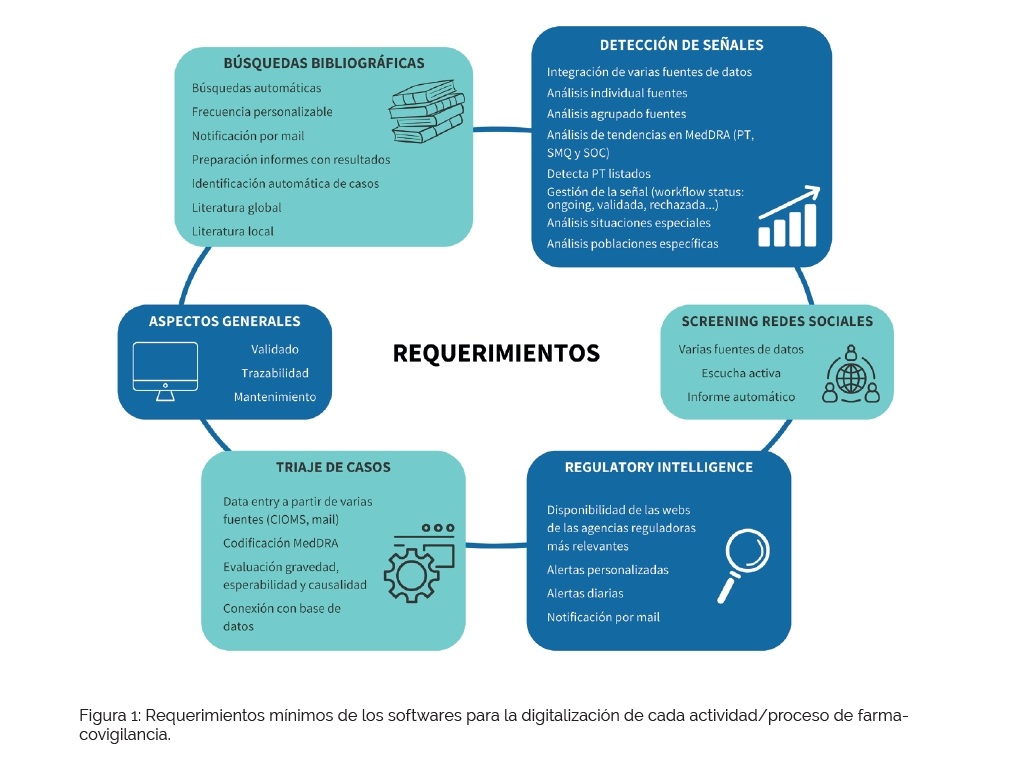
En la figura 1 se muestran los requerimientos mínimos para lo softwares por actividad/proceso de farmacovigilancia.
Modelo de selección de softwares
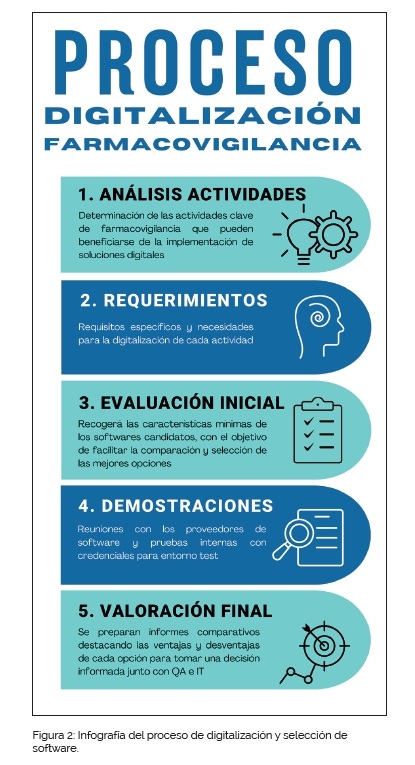
El proceso de análisis y selección de soluciones digitales seguido es el mostrado en la figura 2.
La digitalización de un área de farmacovigilancia comienza con el estudio y el análisis de las actividades que pueden beneficiarse de la digitalización. Una vez identificadas, se establecen los requerimientos específicos y necesidades para la digitalización de cada una de ellas.
Posteriormente, se deben evaluar los diferentes softwares candidatos con el objetivo de hacer una comparación de las prestaciones de cada uno en base a las necesidades y expectativas y con ello facilitar la selección.
Una vez identificados los potenciales softwares, se realiza una evaluación más detallada a través de cuestionarios y demostraciones y se revisa toda la información conjuntamente para chequear el cumplimiento de los requisitos definidos.
A continuación, se preparan informes comparativos que incluyen los resultados de las evaluaciones de los softwares candidatos, destacando las ventajas y desventajas de cada uno de ellos, centrándose en la revisión de, la adaptabilidad, escalabilidad, coste y nivel de soporte ofrecido por el proveedor del software.
Finalmente, se hace una valoración conjunta a nivel de farmacovigilancia, QA e IT para tomar una decisión óptima y comenzar a trabajar con el proveedor para la implementación interna.
Conclusión
La incorporación de IA y la digitalización de las actividades/procesos de farmacovigilancia está redefiniendo el panorama de funcionamiento de esta área y la evaluación de la seguridad de los productos. Estas tecnologías permiten el análisis de grandes volúmenes de datos de manera más rápida y precisa, lo cual mejora la detección de posibles problemas de seguridad y permite una respuesta más rápida. Por su parte, la automatización de tareas rutinarias libera tiempo para que los profesionales de farmacovigilancia se centren en actividades más analíticas, estratégicas y que aportan más valor añadido.
Es importante destacar que se plantean nuevos desafíos, como garantizar la seguridad de los datos y la privacidad del paciente, así como una formación continua para adaptarse a estas nuevas herramientas. A pesar de los desafíos existentes, estos softwares revolucionaran las actividades de farmacovigilancia, beneficiando a los profesionales de la salud y a los pacientes.
Descarga sugerida:
Artículo escrito por:
Sonia López Sánchez y Francisco Rodríguez Lozano
Pharmacovigilance Director/QPPv y Drug Safety Officer, respectivamente
Asphalion