La industria farmacéutica enfrenta una doble transformación, digital y verde, en su camino hacia un modelo más sostenible y competitivo. Este artículo explora el potencial del enfoque Quality by Design (QbD) como catalizador de la transición gemela en el sector. A través de un estudio mixto que combina un análisis bibliométrico con entrevistas a actores clave del ecosistema innovador en España, se analiza cómo QbD puede promover la digitalización y fomentar prácticas sostenibles desde el diseño del producto y proceso.
Con base en estos análisis, se propone un marco conceptual que sugiere que la interiorización de QbD, junto con la integración de sistemas de gestión y una cultura organizacional orientada a la calidad, puede facilitar la incorporación de atributos ambientales en el desarrollo farmacéutico. Asimismo, la colaboración interdisciplinar y la adopción sustantiva de QbD es un factor clave para afrontar los retos regulatorios, tecnológicos y medioambientales en los cambios de procesos de innovación en la industria farmacéutica.
La Industria Farmacéutica (IF) global ha experimentado un notable crecimiento en las dos últimas décadas, alcanzando en 2023 unos ingresos totales cercanos a los 1,47 billones de euros. Esta magnitud sitúa al sector en una dimensión comparable al producto interior bruto de países como España, consolidándose así como uno de los pilares económicos más relevantes a escala mundial [1]. Las empresas farmacéuticas invierten en promedio más del 20% de sus ingresos en Investigación y Desarrollo (I+D) [1], y pese a ello, el sector se enfrenta a grandes retos operacionales en la era de la digitalización [2] relacionados con la calidad con una tendencia al alza del nivel de retiradas de medicamentos o recalls [3]. En paralelo, los fármacos contribuyen alrededor del 3% de las emisiones globales de CO2-equivalente, con un crecimiento del 77% de su huella global de gases de efecto invernadero de la IF entre 1995 y 2019 [4]. Por tanto, la transición gemela, que implica la integración de las transformaciones digital y verde, es uno de los retos fundamentales para lograr un futuro sostenible y competitivo [5].
La digitalización en la IF
La IF, y en especial las Contract Development Manufacture Organizations (CDMO, por sus siglas en inglés), ha sido reticente a la digitalización debido a la complejidad de sus procesos y cadenas de suministro y la limitada experiencia en este ámbito [6]. Sin embargo, la creciente demanda de medicamentos, entre otros factores, hace necesaria su transformación digital, la cual debe alinearse con las Good Manufaturing Practices (GMP, por sus siglas en inglés) y con una colaboración activa con actores cambiantes [2]. Las GMP son obligatorias y aseguran un nivel mínimo de cumplimiento de estándares de eficacia, seguridad y calidad. Por tanto, la calidad juega un papel crítico en los procesos de digitalización en la IF.
La transición verde en al IF
La sostenibilidad en la IF está sujeta a grandes retos, en un entorno en el que un Active Pharmaceutical Ingredient (API) llamado ‘verde’ no significa que no tenga impacto medioambiental, sino que es menos dañino ya sea por su exposición y/o por sus efectos reducidos [7]. Teniendo en cuenta que dichos efectos pueden afectar seriamente a la biodiversidad tras su excreción, es necesario gestionar sus efectos a lo largo de todo el ciclo de vida de estos componentes a partir de su diseño [7], [8]. Así, los conceptos ‘by design’ juegan un papel muy relevante en promover el cumplimiento de sus objetivos subyacentes al ser marcos que se basan en enfoques interdisciplinares que promueven el desarrollo tecnológico juntamente con el cumplimiento regulatorio [9].
El rol de Quality-by-Design (QbD)
Quality-by-Design (QbD), es un marco establecido en la IF, cuya historia en el sector se remonta a 2006 mediante las guías ICH, concretamente la ICH Q8 que fue revisada en 2009. QbD es un enfoque sistemático para el desarrollo que comienza con objetivos predefinidos y enfatiza la comprensión y el control del producto y del proceso, basado en la ciencia y la gestión de riesgos de calidad [10]. Por tanto, su aplicación se encuentra ligada al sistema de gestión de calidad (ICH Q10), gestión de riesgos de calidad (ICH Q9) y la gestión del ciclo de vida del producto (IHC Q12). En un artículo reciente [11], se ha identificado que la implementación de QbD se encuentra en una fase de interiorización a nivel global, y por tanto QbD representa uno de los conceptos ‘by design’ con mayor nivel de implementación en la IF. QbD puede estar relacionada con la digitalización al promover la mejora continua y la innovación radical mediante la implementación de herramientas tecnológicas digitales tales como Process Analytical Technologies (PAT) y Real Time Release Testing (RTRT) [11], [12]. Relacionado con la sostenibilidad, existen varios marcos como la recientemente publicada guía de ‘safe and sustainable by design’ [8]. Pese a su potencial en promover la transición verde, su implementación en la IF aún requiere un mayor nivel de regularización y difusión [8]. Considerando que QbD ya cuenta con estos aspectos, es necesario entender los mecanismos mediante los cuales QbD podría tener un rol relevante en promover la transición gemela, digital y verde.
Metodología
Se realizó un estudio mixto que combina un análisis temático de la literatura con un análisis cualitativo. En cuanto a la primera, se recopilaron los artículos publicados en Web of Science mediante la estrategia de búsqueda siguiente [11]:
Topic = (qbd or "quality-by-design") and "pharma*") and Article or Review Article (Document Types) and English (Languages)
Se llevó a cabo un análisis del mapa de evolución temática en la IF con la ayuda del Software SciMAT [13] para identificar las principales tendencias que relacionen QbD con la transición gemela en la literatura existente.
En cuanto al análisis cualitativo, se realizaron 20 entrevistas a ejecutivos senior de los actores involucrados en el ecosistema de innovación relevantes en España: multinacionales globales, pequeñas y medianas empresas, y universidades [11]. Se realizó un muestreo intencionado, que evita la selección aleatoria para garantizar una muestra final de casos relevantes para el estudio [14]. Se hizo un análisis abductivo, en el que se combinan los datos de las entrevistas con una teoría de compás [15], tomando como teoría los elementos del concepto de Calidad 4.0, el cual está marcado por tres pilares: las personas, la tecnología y los sistemas de gestión [16].
Resultados y Discusión
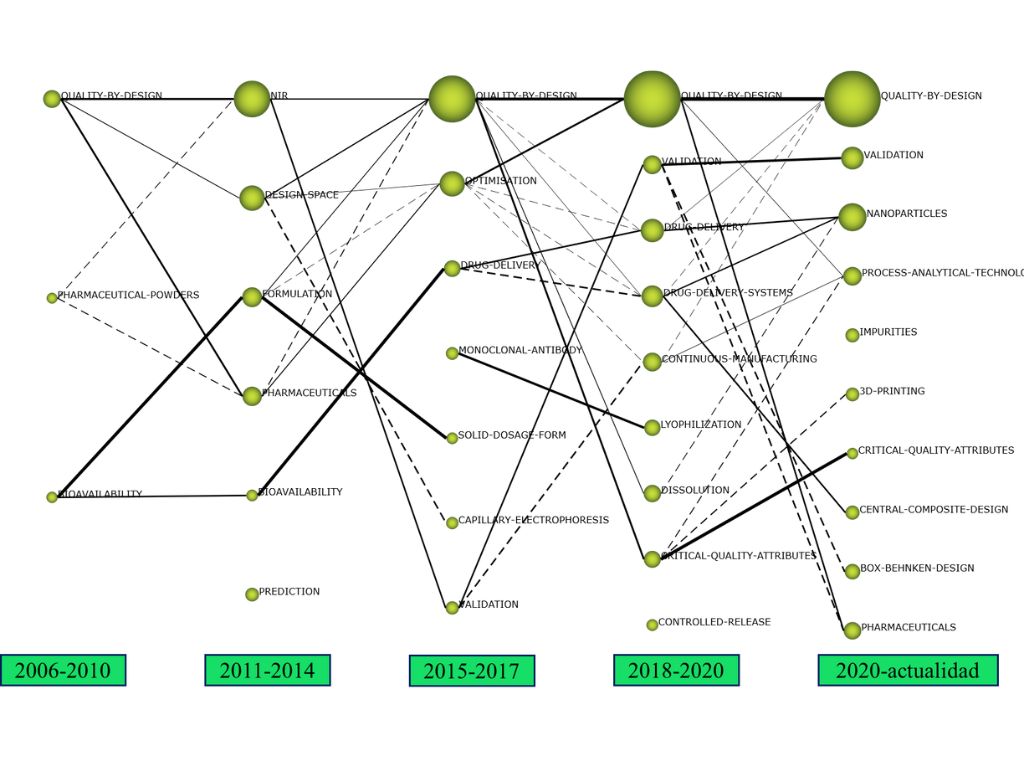
La Figura 1 muestra el mapa de evolución de los temas relacionados en QbD en la literatura especializada en la IF. Aunque tecnologías como PAT o 3D Printing no son nuevas, toman una mayor relevancia como temas motores en la literatura desde 2020 hasta la actualidad. Esto se debe, principalmente, al rol de estas tecnologías en promover la digitalización en procesos de modernización hacia la fabricación continua [12] y explotar los datos mediante el uso de inteligencia artificial [17]. No obstante, no se observa todavía en la literatura el desarrollo de QbD como motor de la transición verde.
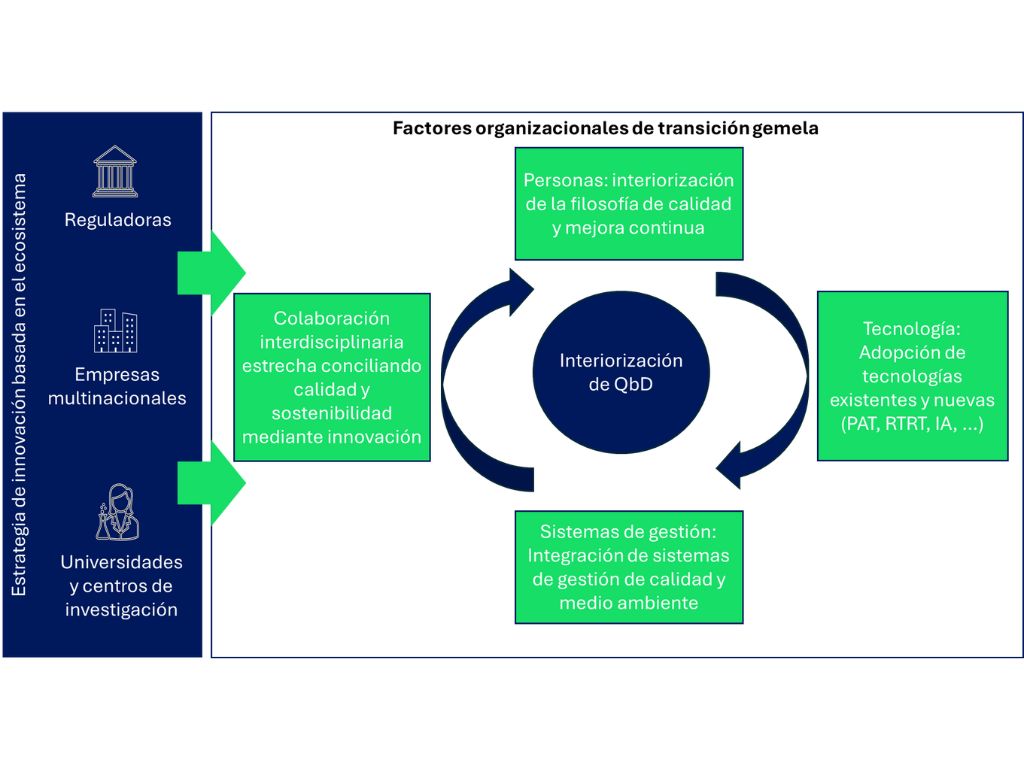
La realización de las entrevistas sugiere patrones similares de adopción de QbD en comparación con los resultados obtenidos anteriormente en relación con la transición digital. No obstante, se observa también que QbD tiene el potencial de integrar la transición verde al incluir parámetros medioambiente como variables a optimizar, por ejemplo, como critical quality attributes (CTAs). La disponibilidad de PAT se da por hecho para esta transición en la mayoría de los casos.
Además, una implementación profunda de QbD en la cultura de las personas, juega un papel relevante. En las organizaciones en las que existe una mayor cultura de calidad en general, y de QbD como concepto, hay una mayor propensión a considerar elementos de sostenibilidad. Pese a ello, se observan barreras organizacionales para que esto ocurra de forma más fluida, mismas que se relacionan con la separación de las funciones de calidad de las de sostenibilidad. Se observa que la integración de los sistemas de gestión que marcan estos procesos facilita la transición gemela, puesto que favorece la adopción de innovaciones organizacionales, el desarrollo e implementación de tecnologías verdes y, a través de ello, innovaciones de productos más sostenibles [18]. Para ello, se observa que la adopción sustantiva (más que simbólica) [19] del concepto de QbD en una filosofía organizativa integrada es fundamental para que se de esta relación de transición gemela.
Finalmente, uno de los factores clave para conseguir implementar estas estrategias de innovación, es la interdisciplinariedad. La integración de reguladoras y la academia en los procesos de innovación son consideradas la ‘salsa secreta’ [12] para la transición gemela, al ser estrategias de innovación basadas en el ecosistema y no solo en una empresa específica [11]. En base a ello, se observan oportunidades en desarrollar conceptos, guías y prácticas pioneras tales como ‘safe and sustainable by design’ [8], las cuales pueden aprovechar el ecosistema y marco regulatorio existente alrededor de QbD para facilitar su integración en la IF.
Los resultados expuestos se resumen en el marco propuesto en la Figura 2.
Aunque la transición digital y verde son cada vez más necesarias en la IF, su implementación tiene varios retos que requieren de un pensamiento sistémico e interiorizado desde el diseño mismo de los procesos, desarrollos e innovaciones. Esto implica ir más allá del compliance, manteniendo la esencia de mejora continua de la calidad. En este artículo, identificamos QbD como un marco de referencia que puede jugar un rol relevante en promover la transición gemela teniendo como base la interdisciplinariedad, la colaboración dentro del ecosistema de innovación, y los pilares de calidad 4.0: personas, tecnología e integración de sistemas de gestión.
Referencias
[1] M. Mikulic, «Global pharmaceutical industry - statistics & facts», Statista. Accedido: 9 de julio de 2025. [En línea]. Disponible en: https://www.statista.com/topics/1764/global-pharmaceutical-industry/
[2] G. Hole, A. S. Hole, y I. McFalone-Shaw, «Digitalization in pharmaceutical industry: What to focus on under the digital implementation process?», Int. J. Pharm. X, vol. 3, p. 100095, dic. 2021, doi: 10.1016/j.ijpx.2021.100095.
[3] P. Callahan, D. Cenziper, y M. Rose, «The FDA Hasn’t Inspected This Drug Factory After 7 Recalls for the Same Flaw, 1 Potentially Deadly», ProPublica. Accedido: 9 de julio de 2025. [En línea]. Disponible en: https://www.propublica.org/article/glenmark-pharmaceuticals-recalls-fda-oversight
[4] R. H. Hagenaars, R. Heijungs, A. De Koning, A. Tukker, y R. Wang, «The greenhouse gas emissions of pharmaceutical consumption and production: an input–output analysis over time and across global supply chains», Lancet Planet. Health, vol. 9, n.o 3, pp. e196-e206, mar. 2025, doi: 10.1016/s2542-5196(25)00028-2.
[5] S. Tabares, V. Parida, y K. Chirumalla, «Twin transition in industrial organizations: Conceptualization, implementation framework, and research agenda», Technol. Forecast. Soc. Change, vol. 213, p. 123995, abr. 2025, doi: 10.1016/j.techfore.2025.123995.
[6] G. Anand, G. P. Ball, J. V. Gray, y U. K. Mukherjee, «Operations Management in the Pharmaceutical Industry», J. Oper. Manag., vol. 71, n.o 3, pp. 302-313, abr. 2025, doi: 10.1002/joom.1365.
[7] R. Vidaurre et al., «Design of greener drugs: aligning parameters in pharmaceutical R&D and drivers for environmental impact», Drug Discov. Today, vol. 29, n.o 7, p. 104022, jul. 2024, doi: 10.1016/j.drudis.2024.104022.
[8] N. Puhlmann, E. Abbate, K. Kümmerer, A. G. Oomen, A. M. J. Ragas, y C. Moermond, «Applicability of the European Commission’s framework on safe and sustainable by design to the pharmaceutical sector», Sustain. Chem. Pharm., vol. 42, p. 101845, dic. 2024, doi: 10.1016/j.scp.2024.101845.
[9] M. Miettinen, «“By Design” and Risk Regulation: Insights from Nanotechnologies», Eur. J. Risk Regul., vol. 12, n.o 4, pp. 775-791, dic. 2021, doi: 10.1017/err.2020.58.
[10] «ICH Q8 (R2) Pharmaceutical development - Scientific guideline | European Medicines Agency (EMA)». Accedido: 14 de julio de 2025. [En línea]. Disponible en: https://www.ema.europa.eu/en/ich-q8-r2-pharmaceutical-development-scientific-guideline
[11] A. Hernandez-Vivanco, V. Vlaisavljevic, L. Gonzalez-Moragas, y M. Santana, «Quality-by-design as the pharmaceutical innovation paradigm: mapping the field and proposing a conceptual framework», Technol. Forecast. Soc. Change, vol. 217, p. 124182, ago. 2025, doi: 10.1016/j.techfore.2025.124182.
[12] J. S. Srai, T. S. Harrington, N. R. Joglekar, y S. Narayanan, «Convergence of Product, Production, and Supply Chain Design Rules: Evidence From Pharmaceutical Pre‐Competitive Collaboration Networks», J. Oper. Manag., vol. 71, n.o 3, pp. 314-334, abr. 2025, doi: 10.1002/joom.1352.
[13] M. J. Cobo, A. G. López-Herrera, E. Herrera-Viedma, y F. Herrera, «SciMAT: A new science mapping analysis software tool», J. Am. Soc. Inf. Sci. Technol., vol. 63, n.o 8, pp. 1609-1630, ago. 2012, doi: 10.1002/asi.22688.
[14] S. Merriam, Qualitative research: a guide to design and implementation. Hoboken, NJ, USA: Sage, 2009.
[15] M. B. Miles y A. M. Huberman, Qualitative data analysis: An expanded sourcebook. SAGE, 1994.
[16] A. M. Dias, A. M. Carvalho, y P. Sampaio, «Quality 4.0: literature review analysis, definition and impacts of the digital transformation process on quality», Int. J. Qual. Reliab. Manag., vol. 39, n.o 6, pp. 1312-1335, may 2022, doi: 10.1108/ijqrm-07-2021-0247.
[17] P. Suriyaamporn, B. Pamornpathomkul, P. Patrojanasophon, T. Ngawhirunpat, T. Rojanarata, y P. Opanasopit, «The Artificial Intelligence-Powered New Era in Pharmaceutical Research and Development: A Review», AAPS PharmSciTech, vol. 25, n.o 6, ago. 2024, doi: 10.1208/s12249-024-02901-y.
[18] A. Hernandez-Vivanco, M. Bernardo, y C. Cruz-Cázares, «Sustainable innovation through management systems integration», J. Clean. Prod., vol. 196, pp. 1176-1187, sep. 2018, doi: 10.1016/j.jclepro.2018.06.052.
[19] K. Iatridis y E. Kesidou, «What Drives Substantive Versus Symbolic Implementation of ISO 14001 in a Time of Economic Crisis? Insights from Greek Manufacturing Companies», J. Bus. Ethics, vol. 148, n.o 4, pp. 859-877, abr. 2018, doi: 10.1007/s10551-016-3019-8.
Artículo escrito por:
Alfonso Hernandez-Vivanco | Vesna Savic
Profesor contratado doctor | Profesora lectora
IQS School of Management, Universidad Ramon Llull